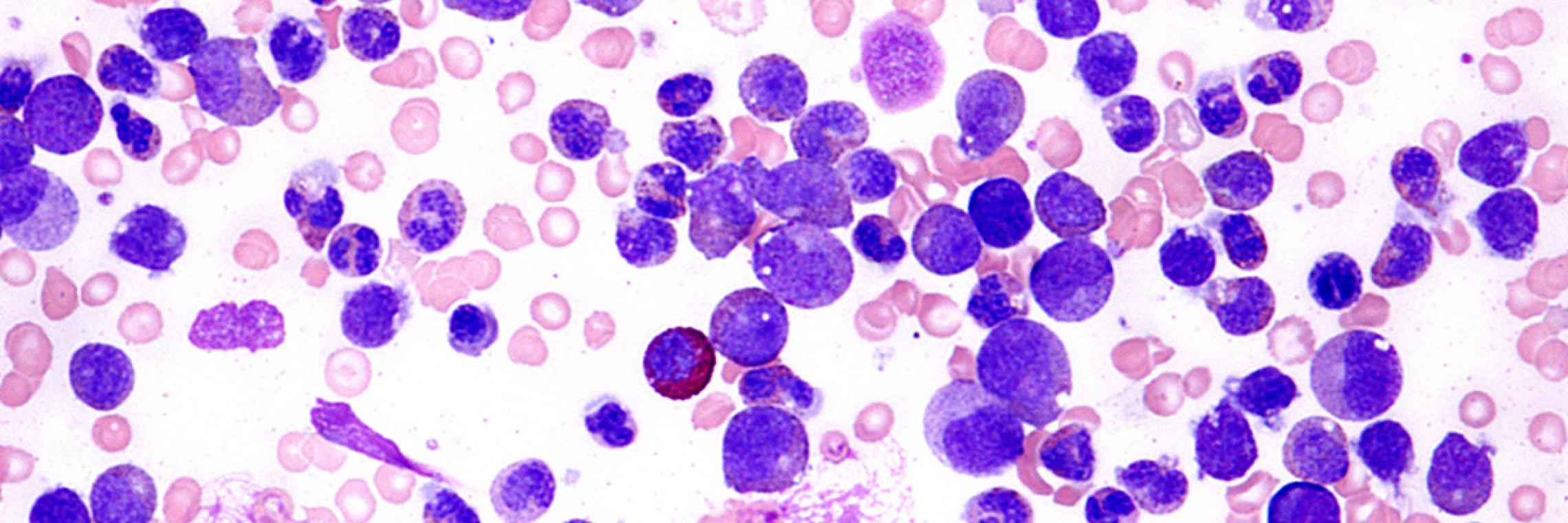
Die Behandlungsoptionen umfassen Chemotherapie, Stammzelltransplantation, Bestrahlung sowie auch die Gabe neuer Wirkstoffe (Antikörper, Immunmodulatoren, Proteasominhibitoren). Welche Therapie in Frage kommt, muss individuell festgelegt werden und hängt vom Krankheitsstadium sowie vom Alter und Allgemeinzustand der Patientin oder des Patienten ab.
- Als Methode der Wahl gilt aktuell die Hochdosischemotherapie mit nachfolgender autologer Stammzelltransplantation (ASZT). Eine obere Altersgrenze für diese Behandlungsoption ist schwer zu definieren, jedoch ist ein ausreichend guter körperlicher Allgemeinzustand als Voraussetzung für diese Behandlungsoption anzusehen
- Die Kombination konventioneller und neuer Wirksubstanzen (z. B. Zytostatika, Kortikosteroide, immunmodulierende Wirkstoffe, Proteasominhibitoren, Antikörper,) hat zu einer bedeutenden Verbesserung der Behandlungsergebnisse geführt, sowohl in der Induktionstherapie vor Hochdosistherapie und ASZT, als auch bei der Behandlung nicht für Hochdosistherapie/ASZT geeigneter Patient:innen
- Monotherapien der Wirksubstanzen können als Erhaltungstherapie bei Patient:innen nach ASZT eingesetzt werden.