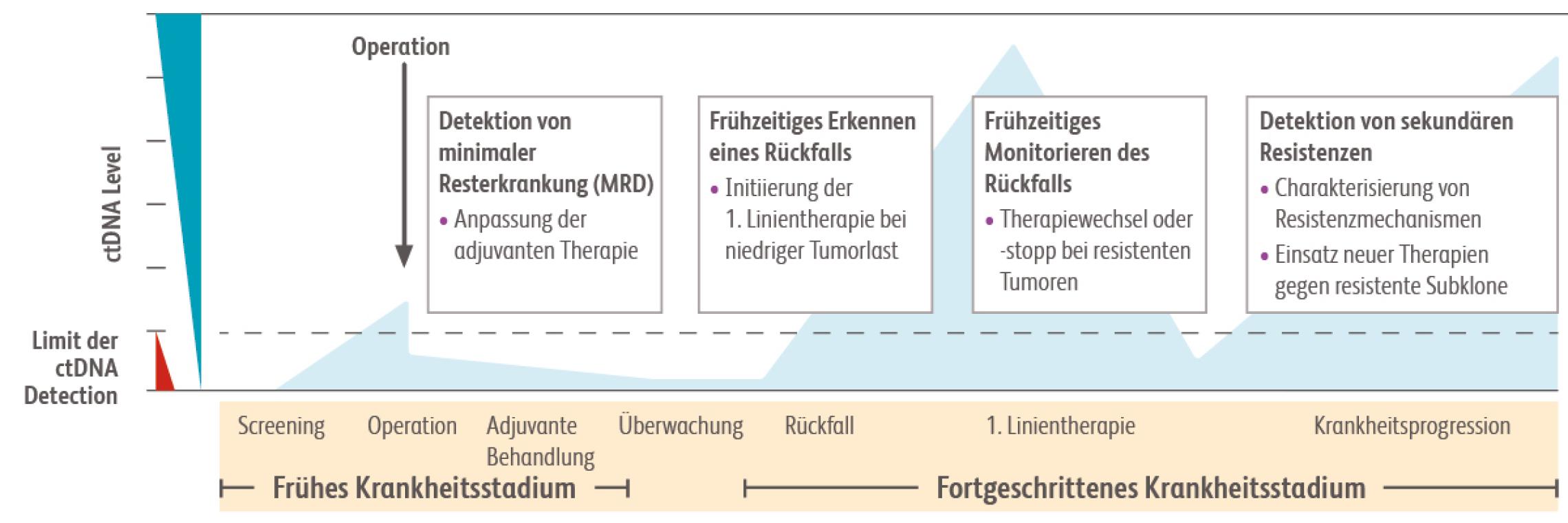
Insbesondere für den adjuvanten Therapiebereich wird die Verlaufskontrolle von Krebserkrankungen mittels Liquid Biopsy als besonders wichtig erachtet. Soll das Ansprechen auf eine adjuvante Therapie beurteilt werden, ist man mit den herkömmlichen bildgebenden Methoden nach der Tumorresektion weitestgehend „blind“. Erst wenn ein Rezidiv im CT erkennbar ist, kann eine Entscheidung zur Therapieänderung getroffen werden. Die ctDNA birgt daher besonders im adjuvanten Bereich das Potenzial als hochsensitiver Marker zur Verlaufskontrolle und Beurteilung von MRD (minimal residual disease) zu fungieren. Die Quantifizierung von ctDNA nach der operativen Entfernung des Tumors sowie im weiteren Verlauf ermöglicht es, das Ansprechen auf eine adjuvante Therapie kontinuierlich zu überprüfen und ein Rezidiv frühzeitig zu erkennen. Durch den Nachweis von ctDNA ist es also möglich eine Therapieänderung einzuleiten, bevor ein Rezidiv in der Bildgebung sichtbar wird.Bei der hier gewonnen Zeit, spricht man auch von Lead Time.
Aber auch im metastasierten Stadium hat das kontinuierliche Messen der ctDNA-Konzentration das Potenzial, das Ansprechen oder die Resistenzentwicklung auf eine Therapie zu detektieren. Hypothetisch wird ctDNA nicht nur von Zellen des Primärtumors, sondern auch von neuen, resistenten Subklonen abgegeben. Die ctDNA-Analyse bietet also die Chance, ein umfassenderes genetisches Bild des Tumors zu erhalten, als es mit punktueller Gewebebiopsie der Fall ist.Mit dieser Information ist dann nicht nur die Verlaufskontrolle möglich, sondern auch die Anpassung der Therapie an die entwickelte Resistenz (Behandlungssequenzen).
Die ctDNA birgt damit das Potenzial, als Marker für die Verlaufskontrolle einer Therapie im adjuvanten sowie metastasierten Stadium zu fungieren. Daher ist dieser Ansatz auch Gegenstand der aktuellen Forschung bei Bristol Myers Squibb und wird in klinischen Studien untersucht.