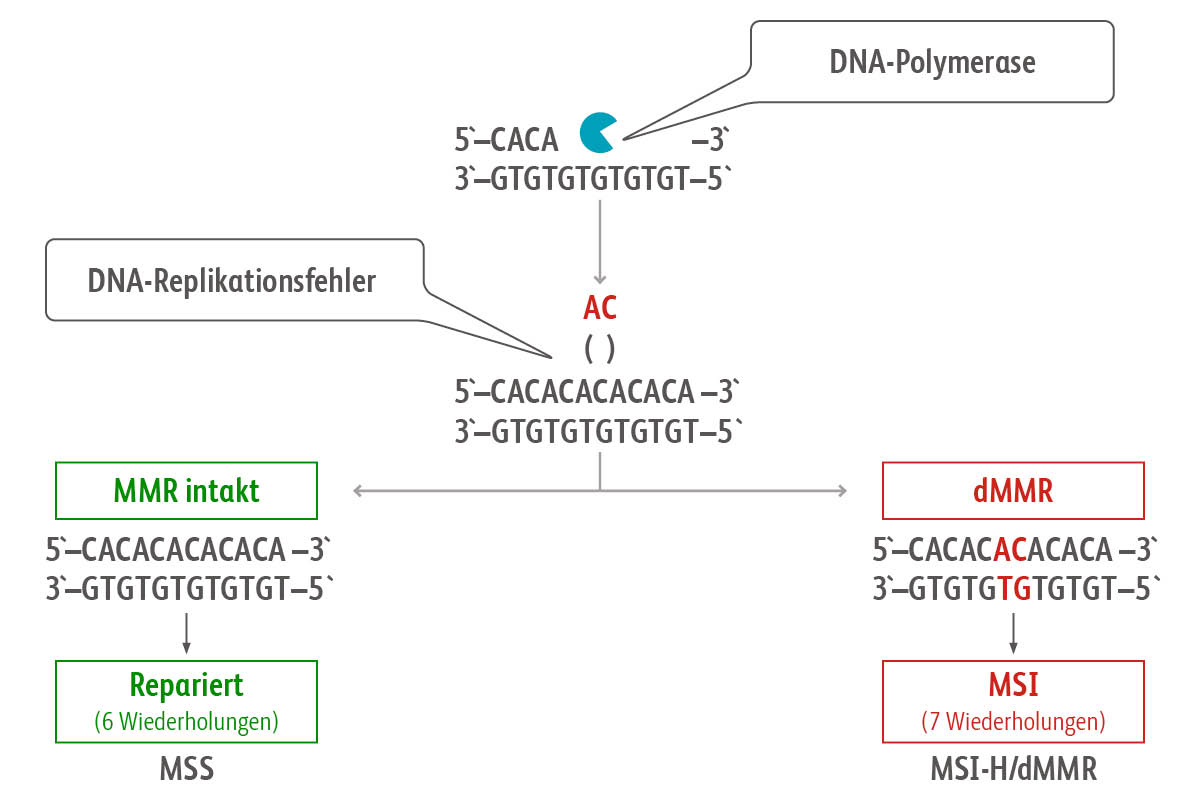
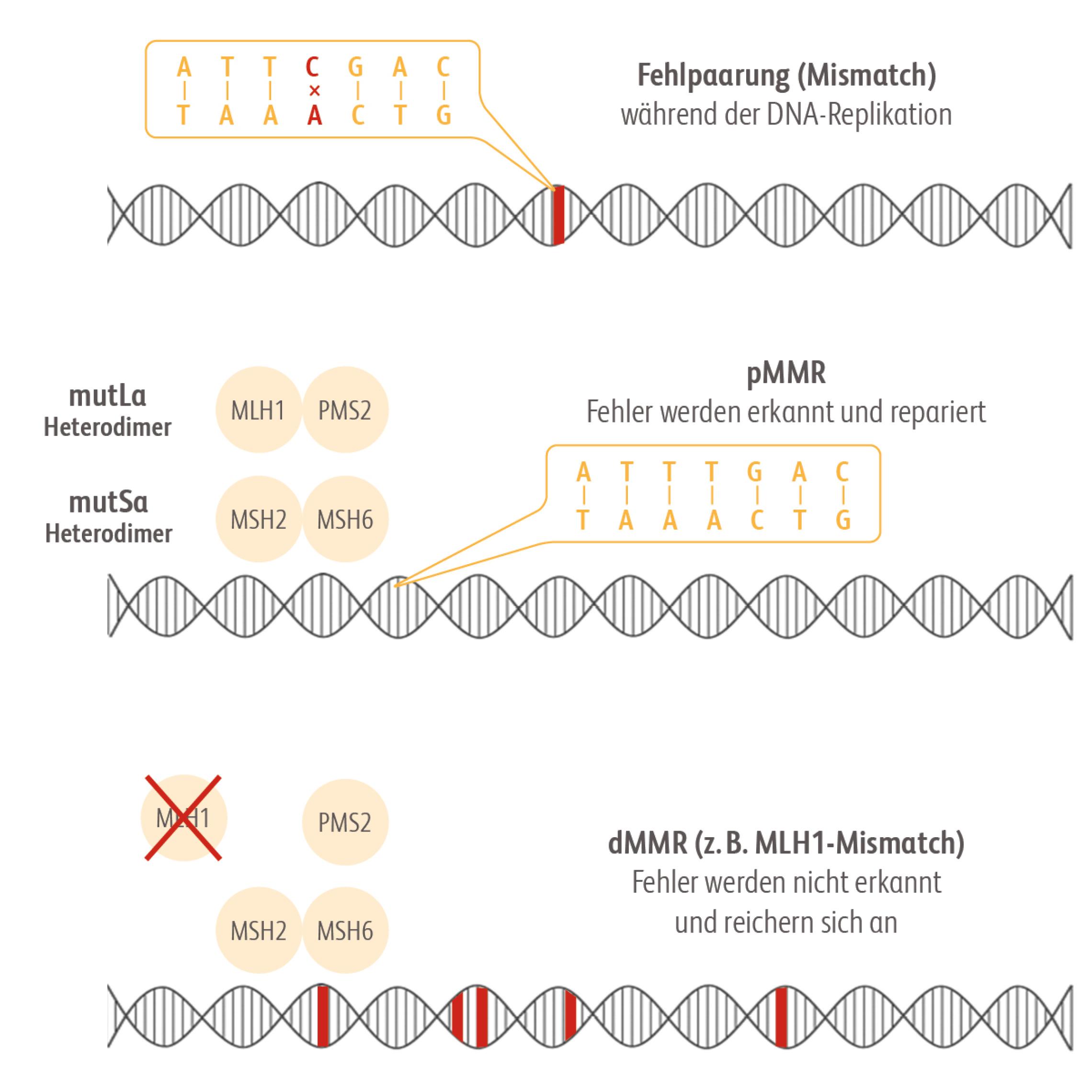
Sind eines oder mehrere Gene des Mismatch-Reparatur-Systems defekt oder durch Hypermethylierung inaktiv, bezeichnet man dies als dMMR (deficient MMR).Richman S. Deficient mismatch repair: Read all about it (Review). Int J Oncol. 2015;47(4):1189-202. doi:10.3892/ijo.2015.3119dMMR kann zu einer Anhäufung von Mutationen führen, insbesondere in den Bereichen der Mikrosatelliten.Richman S. Deficient mismatch repair: Read all about it (Review). Int J Oncol. 2015;47(4):1189-202. doi:10.3892/ijo.2015.3119
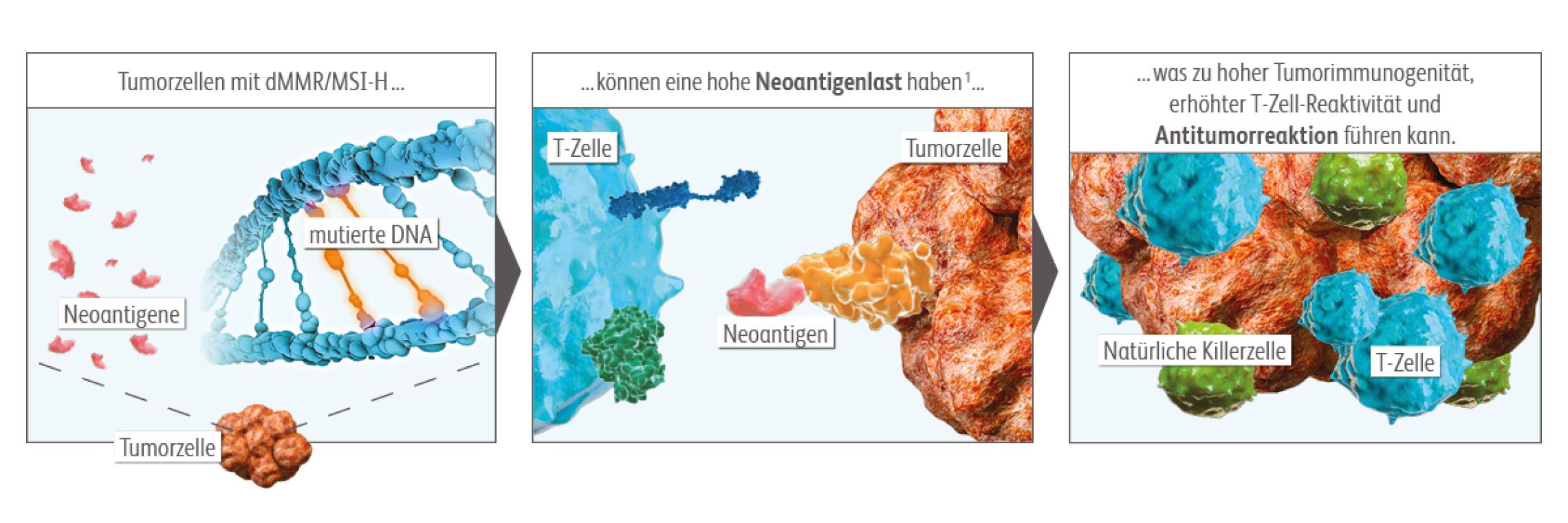
Eine Anhäufung von Mutationen in diesen Mikrosatelliten wird als hohe Mikrosatelliteninstabilität (MSI-H) bezeichnet. Die Mutationen können kodierende Regionen der DNA direkt oder indirekt beeinflussen.Kawakami H, Zaanan A, Sinicrope FA. Microsatellite instability testing and its role in the management of colorectal cancer. Curr Treat Options Oncol. 2015;16(7):30. doi:10.1007/s11864-015-0348-2 Lee V, Murphy A, Le DT, Diaz LA, Jr. Mismatch Repair Deficiency and Response to Immune Checkpoint Blockade. Oncologist. 2016;21(10):1200-1211. doi:10.1634/theoncologist.2016-0046Dies führt dazu, dass dMMR/MSI-H-Tumore insgesamt eine Vielzahl von Mutationen und somit eine hohe TumormutationslastKawakami H, Zaanan A, Sinicrope FA. Microsatellite instability testing and its role in the management of colorectal cancer. Curr Treat Options Oncol. 2015;16(7):30. doi:10.1007/s11864-015-0348-2 Lee V, Murphy A, Le DT, Diaz LA, Jr. Mismatch Repair Deficiency and Response to Immune Checkpoint Blockade. Oncologist. 2016;21(10):1200-1211. doi:10.1634/theoncologist.2016-0046 Le DT, Uram JN, Wang H, et al. PD-1 Blockade in Tumors with Mismatch-Repair Deficiency. N Engl J Med. 2015;372(26):2509-20. doi:10.1056/NEJMoa1500596sowie eine höhere Anzahl an Neoantigenen aufweisen.Schumacher TN, Schreiber RD. Neoantigens in cancer immunotherapy. Science. 2015;348(6230):69-74. doi:10.1126/science.aaa4971