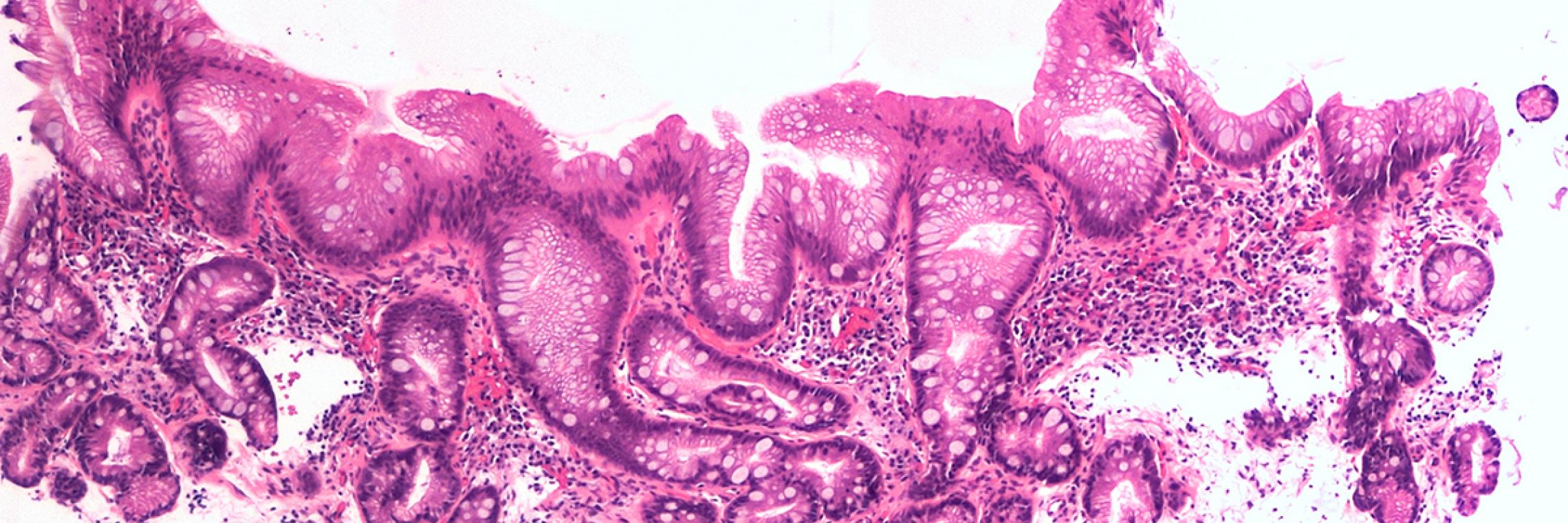
Ösophaguskarzinome machen rund 1 % aller malignen Tumorerkrankungen aus und sind damit vergleichsweise selten. Sie manifestieren sich in der Regel als Adeno- oder Plattenepithelkarzinome und je nach Lokalisation sowie Lagebeziehung innerhalb des Brustkorbs unterscheidet man zervikale, und intrathorakale Tumoren.Deutsche Gesellschaft für Hämatologie und Medizinische Onkologie e.V. Onkopedia. Ösophaguskarzinom. Stand 2018. https://www.onkopedia.com/de/onkopedia/guidelines/oesophaguskarzinom/@@guideline/html/index.html; abgerufen am 28.07.2020.